
CeO2-活性炭催化臭氧化降解水中草酸的研究
摘要:
利用CeO2的储氧和释氧能力,以高活性的活性炭作为催化剂载体,采用等体积浸渍法制备CeO2-活性炭催化剂。分别用氮气低温吸附/脱附、XRD、XPS对CeO2-活性炭催化剂进行表征。以CeO2-活性炭作为催化剂,草酸作为模型化合物,催化臭氧化降解草酸的去除率达到77%。Ce组分的加入能显著提高草酸的去除率。Ce不仅能够提高反应体系中羟基自由基的浓度,还有利于O3分子直接氧化草酸。CeO2-活性炭催化剂经过3次重复使用后,草酸去除率保持在70%以上,具有较好的稳定性。
草酸是一种重要的化工原料,广泛应用于医药、化工等领域〔1〕 。草酸也是多种有机物污染物经臭氧催化氧化处理后的难降解中间产物,和有机污染物的矿化程度直接相关〔2〕 。因此,臭氧催化氧化反应中草酸去除率的高低与催化剂活性密切相关。
臭氧催化氧化反应是利用催化剂提高臭氧的利用率,促进O3产生更多的羟基自由基,加快对有机物的分解速度。研究表明,活性炭(AC)能加速O3的分解产生·OH。U.Jans等〔3〕 向含O3的溶液中添加微量活性炭或炭黑能明显加快O3分解生成·OH的速率,12 min内O3的分解率提高到88.9%。F.J.Beltrán等〔4〕 对活性炭催化分解臭氧动力学的研究也证实,活性炭可加快O3在水溶液中的分解速率。此外,金属氧化物也被证实能提高O3对有机污染物的降解能力,如Ti O2〔5〕 、Fe2O3〔6〕 、Mn O2〔7〕 、Co3O4〔8〕 等均能提高O3对草酸的去除率。
近年来,含Ce O2材料逐渐应用到很多领域,如发光材料、光催化、紫外吸收材料、汽车尾气净化催化剂等〔9〕 ,但将Ce O2应用于水中草酸的研究还鲜有报道。相对于已经报道的金属氧化物,Ce O2是一种N型半导体,具有较强的氧化还原能力,Ce很容易在Ce3+和Ce4+间转换,具有较高的储氧和释氧能力,当Ce O2经过高温处理后,易造成氧缺位,形成潜在的活性中心。
笔者采用活性炭作为载体,以硝酸铈作为前驱体,采用等体积浸渍法制备了Ce O2-活性炭(Ce O2-AC)催化剂。利用AC和铈氧化物的协同作用,提高对草酸的去除率,并对Ce O2-AC催化臭氧化降解草酸的机理进行了研究。
1 试验部分
1.1 试剂与仪器
活性炭购于山西华瑞活性炭有限公司;Ce(NO3)3·6H2O、草酸等试剂均为分析纯。
SSA-4200比表面积测定仪,彼奥德电子技术有限公司;KTL型管式炉,南京南大仪器有限公司;NS-110X30水浴恒温摇床,上海世平实验设备有限公司;p HS-25型酸度计,成都方舟科技开发公司;FA2004N型电子天平,上海民桥精密科学仪器有限公司;UV-2000型紫外可见分光光度计,尤尼柯仪器有限公司;台式COD测定仪,北京双晖京承电子产品有限公司;臭氧发生器,;Agilent 1100高效液相色谱仪,安捷伦科技有限公司。
1.2 催化剂的制备
活性组分铈前躯体为Ce(NO3)3·6H2O,在不断搅拌下逐滴加入到适量的活性炭(0.15~0.074 mm,100~200目)中,采用等体积浸渍法浸渍过夜,100℃干燥后,于管式炉中在300℃下煅烧2 h后降至室温,整个煅烧过程均在氮气保护下进行,氮气流量为60 m L/min。
1.3 催化剂的表征
1.3.1 比表面积和孔径分布
活性炭载体和催化剂样品的孔结构测试在NOVA 2200e型氮气吸附仪上进行,样品的比表面积通过BET方程计算,总的孔体积通过氮气在相对压力为0.99时的吸附量转换为相应体积获得;中孔体积、中孔的比表面积和孔径分布通过BJH方法测得。
1.3.2 粉末X射线衍射(XRD)
XRD测试由X’pert pro MPO X射线衍射仪(荷兰飞利浦公司)进行。测试条件:Cu靶(Kα),扫描角度:5~70°。加速电压40 k V,管电流35 m A,扫描速度为0.15(°)/s,扫描步幅为0.3°。
1.3.3 X射线光电子能谱(XPS)
XPS表征在Kratos XSAM800型X射线光电子能谱仪上进行,采用Al KαX射线作为激发源,光子能量为1 486.6 e V;靶功率为250 W,电压12.5 k V;化学位移的校正采用内标法,以有机污染碳的C1s的标准结合能284.6 e V为基准进行校准。
1.4 草酸的催化臭氧化试验
草酸催化臭氧化试验在2 L玻璃反应釜中进行,草酸溶液体积1.5 L,初始质量浓度为500 mg/L,催化剂用量为250 mg/L。氧气经过臭氧发生器产生O3,氧气流量为200 m L/min,O3进入反应器的质量浓度为40 mg/L,O3经过玻璃反应器底部的气体分布装置与溶液鼓泡接触。溶液中草酸的测定采用高效液相色谱进行分析,色谱柱为C18XDB(5μm,4.6 mm×150 mm);DAD检测器(波长254 nm);V(乙腈)∶V〔磷酸溶液(p H=3)〕为10∶90。草酸的剩余率按照式(1)计算。

式中:X———草酸的剩余率,%;
C———草酸任意时刻的质量浓度,mg/L;
C0———草酸的初始质量浓度,mg/L。
2 结果与讨论
2.1 催化剂的表征
2.1.1 活性炭和催化剂的孔结构
活性炭(AC)和Ce O2-AC催化剂的比表面积和孔体积参数见表1。
表1 AC和Ce O2-AC催化剂的孔结构参
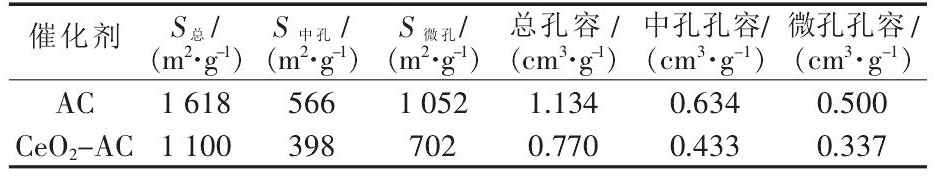
由表1可见,催化剂Ce O2-AC的比表面积为1 100 m2/g,孔体积为0.770 cm3/g。和活性炭相比,中孔和微孔的比表面积分别下降了30%和33%。考虑到煅烧温度较低,对活性炭的孔结构影响较小,因此Ce O2-AC的比表面积和孔体积下降主要是Ce O2颗粒同时进入了活性炭的微孔和中孔造成的。活性炭载体和催化剂Ce O2-AC的孔径分布如图1所示。

图1 活性炭和Ce O2-AC的孔径分布
活性炭表面负载Ce后,在孔径4 nm处的峰高和峰面积明显下降,这表明Ce O2-AC催化剂的比表面积和孔体积比活性炭载体小。
2.1.2 粉末X射线衍射(XRD)
有文献报道活性炭负载Ce O2催化剂的特征衍射峰分别位于28.5°、33.1°、47.5°、56.3°、59.0°〔10〕 。催化剂Ce O2-AC在28.5°和47.5°有明显的衍射峰,但在33.1°、56.3°以及59.0°未出现明显的衍射峰。这可能是催化剂中Ce的负载量过低造成的〔11〕 。当Ce的负载量低于10%,仅仅出现2个峰(28.5°、47.5°),当Ce的负载量超过10%后,28.5°、47.5°、56.3°均会出现特征衍射峰。为进一步确认Ce在催化剂载体表面的存在,采用XPS分析Ce在活性炭载体表面的含量,同时表征Ce在活性炭表面的存在形式。
2.1.3 催化剂X射线光电子能谱(XPS)
Ce O2-AC催化剂的Ce XPS谱图如图2所示。
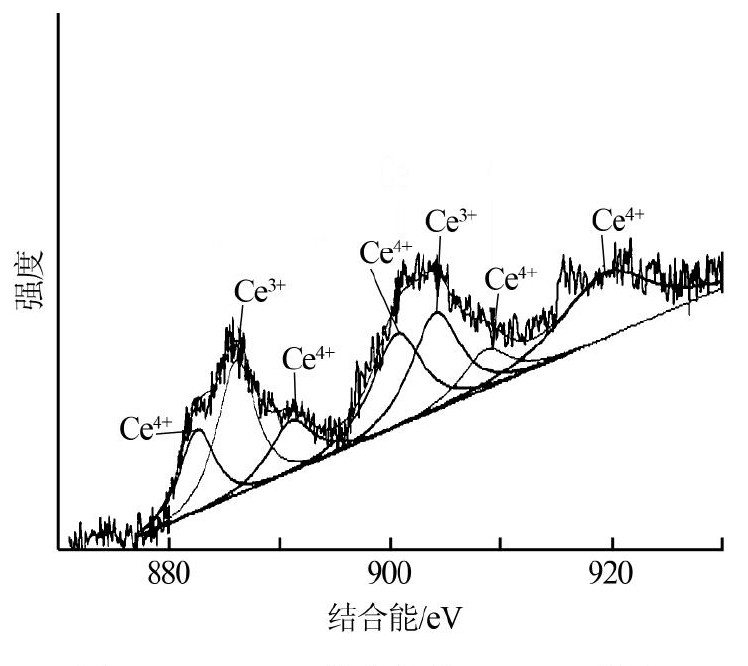
图2 Ce O2-AC催化剂的Ce XPS谱图 Download the original image.
根据文献〔12〕 ,Ce 3d XPS谱图可以拟合出7个峰,Ce3+的峰对应的结合能为886.28、904.02 e V,Ce4+对应的峰分别为883.60、889.71、889.25、901.04 e V,结合能在917 e V处被认为是Ce O2。活性炭表面Ce的存在形式有Ce3+和Ce4+,其中Ce3+的质量分数为36.3%,Ce4+占Ce总量的63.7%。这说明采用等体积浸渍后,经过300℃煅烧可以向活性炭的表面同时引入Ce3+和Ce4+,且催化剂表面主要以Ce4+的形式存在。
2.2 草酸的催化臭氧化试验
草酸臭氧化、AC和Ce O2-AC催化剂对草酸的吸附以及AC、Ce O2-AC催化臭氧化降解草酸过程中,任意时刻的草酸剩余率随时间的变化曲线如图3所示。
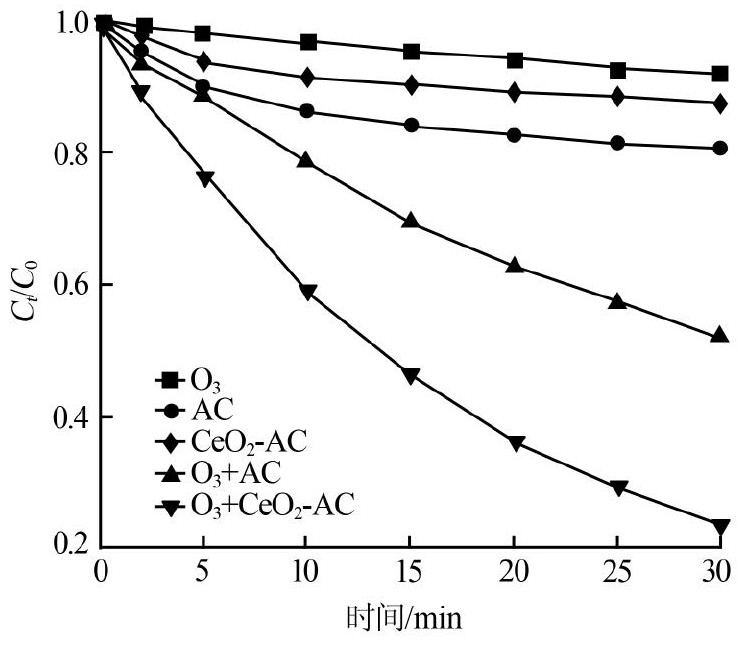
图3 吸附、臭氧化、催化臭氧化过程中草酸剩余率
从草酸的臭氧化降解曲线可以看出:反应30 min后C/C0约为0.97,说明单独使用O3对草酸的降解能力十分有限。比较AC和Ce O2-AC的吸附曲线,AC的吸附量稍高于Ce O2-AC,这主要是因为在Ce O2-AC催化剂的制备过程中,Ce O2颗粒进入到AC的微孔和中孔中,造成Ce O2-AC的比表面积降低。因此Ce O2-AC对草酸的吸附能力要低于AC。由图3可知,单独臭氧化及吸附过程并不能有效去除草酸。
分别以AC、Ce O2-AC作为催化剂,采用催化臭氧化降解草酸时,30 min后草酸剩余率分别达到53%、27%,表明AC和Ce O2-AC能显著提高O3对草酸的降解能力;并且相比AC,Ce O2-AC作催化剂时对草酸的去除率提高了26%,可见Ce能提高对草酸的去除效果。
对S.Avramescu等〔13〕 提出的臭氧催化降解草酸的动力学方程进行积分,可得:

式中:CB———草酸的质量浓度,mg/L;
kt———草酸氧化反应的总速率常数,min-1。
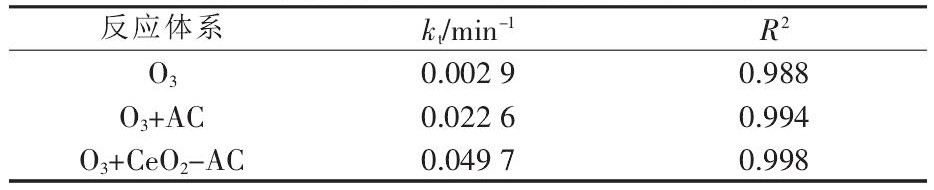
由式(2)可知草酸的催化臭氧化反应属于一级动力学,ln(CBt/CB0)与t呈线性关系,直线的斜率即为总速率常数。对单独臭氧化、AC和Ce O2-AC催化臭氧化草酸的ln(CBt/CB0)~t关系作图,见图4。3个反应体系下的总速率常数(kt)和拟合的线性相关系数(R2)见表2。
由表2可见O3+Ce O2-AC催化体系的总速率常数是O3+AC催化体系的2倍多,说明Ce O2-AC催化剂具有较好的催化活性。
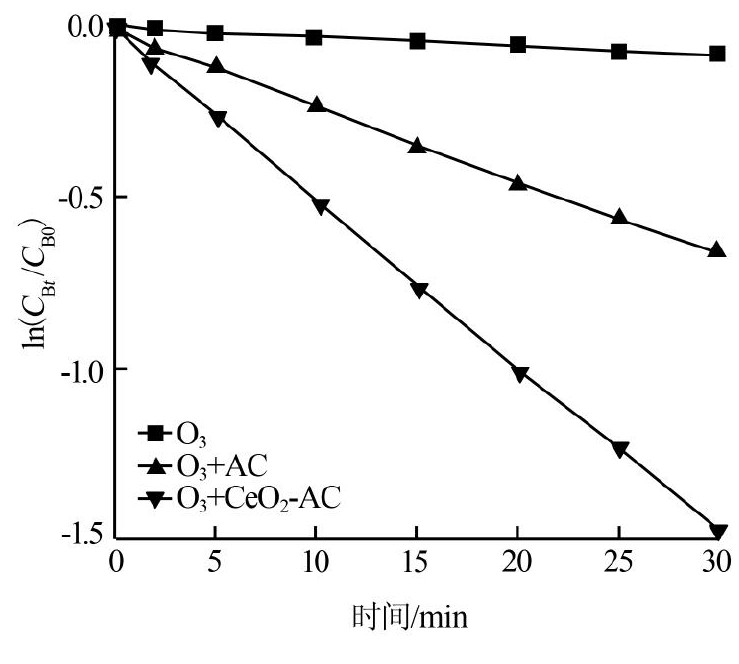
图4 单独臭氧化、AC和Ce O2-AC催化臭氧化草酸的ln(CBt/CB0)~t
表2 草酸降解的一级动力学拟合结果
2.3 叔丁醇对草酸去除率的影响
在催化臭氧化降解有机物的过程中,O3分子与草酸反应的同时,溶液中的自由基也会与草酸反应〔14〕 。向反应溶液中加入叔丁醇能淬灭反应过程中产生的自由基〔15〕 。考察了单独臭氧化、AC催化臭氧化及Ce O2-AC催化臭氧化过程中叔丁醇对草酸浓度的影响,见图5。
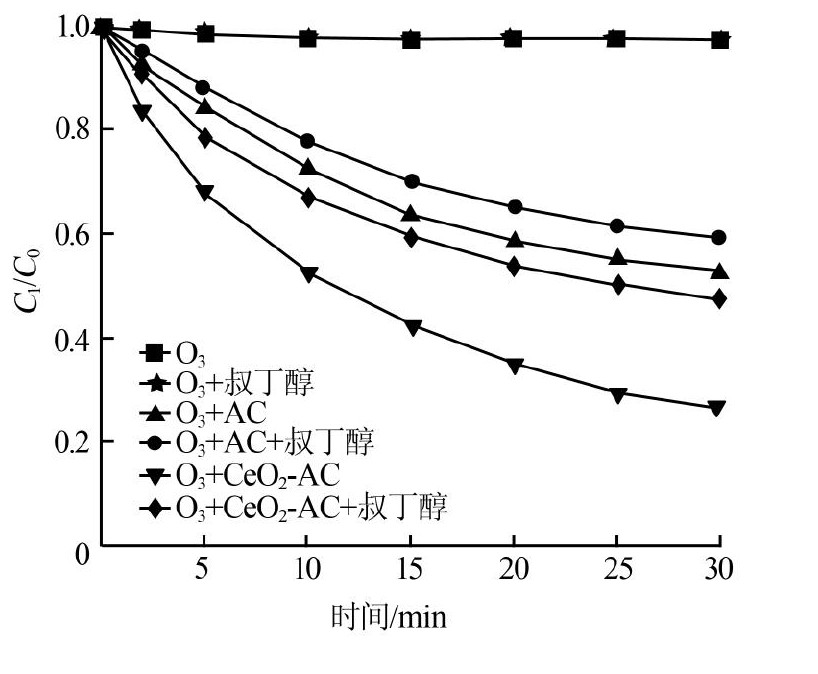
图5 叔丁醇对草酸去除效果的影响
如图5所示,对于单独臭氧化过程,叔丁醇的加入对草酸的降解基本没有影响。对于AC臭氧化过程,添加叔丁醇后,草酸剩余率明显增加,但仍然达到60%。因此,活性炭表面的活化O3分子与草酸之间的反应是草酸降解的主要途径〔16〕 。对于Ce O2-AC催化臭氧化过程,叔丁醇的加入造成草酸剩余率由27%增加到48%,表明草酸降解过程中有自由基参与,此外O3分子的直接氧化过程也具有重要作用。由此可见,Ce组分的添加不仅增加溶液中自由基浓度,还能够提高O3直接氧化草酸的能力。
2.4 温度对草酸去除率的影响
不同温度下AC和Ce O2-AC催化臭氧化降解草酸的效果如表3所示。
表3 反应温度对草酸去除效果的影响

由表3可见,反应温度的增加有利于草酸的去除,这主要是由于温度升高提高了反应动力学常数。此外,当温度从20℃升高到30℃,草酸的降低幅度要高于30℃增加到40℃的幅度,这是O3的溶解度随温度的升高而逐渐减小引起的。因此,过高的温度并不利于草酸的催化臭氧化反应。
2.5 溶液p H对草酸去除率的影响
不同初始p H条件下AC和Ce O2-AC催化臭氧化降解草酸的效果如图6所示。

图6 溶液p H对草酸去除效果的影响
由图6可见,随着溶液p H的增加,AC和Ce O2-AC降解草酸的能力均呈现先逐渐增加后减小的趋势。这与草酸分子在溶液中的存在形式以及催化剂表面电荷性质变化有关。草酸的两级解离常数分别为1.2、4.2。当溶液p H>1.2时,草酸发生一级电离,当溶液p H>4.2时,草酸完全解离成草酸根。
当溶液p H<3时,随着溶液p H的增加,更多的草酸发生一级电离,此时催化剂表面带正电荷,在静电引力作用下,大量草酸阴离子吸附在催化剂表面,造成草酸剩余率较小。当溶液p H继续增加,溶液中出现更多的草酸根离子,与此同时,由于p H的增加造成催化剂表面逐渐由正电荷变为负电荷,在静电斥力作用下,吸附在催化剂表面的草酸离子逐渐减少,造成草酸剩余率增加。此外,O3分子在较高p H溶液中更易分解也是造成草酸剩余率较高的一个原因。
2.6 Ce O2-AC催化剂的重复使用
在应用过程中,催化剂会发生活性组分溶出、催化剂表面活性位点破坏等问题,这会导致催化剂的活性显著降低。为考察Ce O2-AC催化剂的重复使用性能,每次实验结束后过滤催化剂,重新加入到新鲜草酸溶液中进行重复试验。结果发现,催化剂重复使用3次后草酸剩余率稍有增加,但草酸剩余率均<30%,表明Ce O2-AC催化剂的稳定性较好。
3 结论
(1)向AC表面引入Ce组分制备出的Ce O2-AC催化剂在草酸催化臭氧化反应中表现出较高的活性,Ce O2-AC对草酸的去除率约为77%,比AC反应体系高30%;Ce O2-AC降解草酸的动力学速率常数是AC反应体系的2倍多。Ce O2-AC催化剂的高活性主要是由于Ce在提高溶液中自由基浓度的同时,也促进O3与草酸分子直接发生氧化反应。
(2)温度升高有利于草酸剩余率的降低,但由于O3溶解度的原因,过高的温度不利于O3对草酸的降解。p H会影响草酸分子在溶液中的存在形式和催化剂表面电荷性质,当溶液p H为3时,Ce O2-AC催化剂的活性很高。Ce O2-AC催化剂重复使用3次后,草酸去除率仍高于70%,Ce O2-AC催化剂具有较好的稳定性。
References
[1]王龙耀,王丽娟,王岚.改性活性白土负载Fe(Ⅱ)催化臭氧化去除草酸的研究[J].工业水处理,2014,34(3):43-46.
[2]Beltrán F J,Rivas F J,Montero-de-Espinosa R.A Ti O2/Al2O3catalyst to improve the ozonation of oxalic acid in water[J].Applied Catalysis B:Environmental,2004,47(2):101-109.
[3]Jans U,HoignéJ.Activated carbon and carbon black catalyzed transformation of aqueous ozone into OH-radicals[J].Ozone Science&Engineering,1998,24(1):67-90.
[4]Beltrán F J,Rivas J,lvarez P,et al.Kinetics of heterogeneous catalytic ozone decomposition in water on an activated carbon[J].Ozone Science&Engineering,2002,24(4):227-237.
[5]Beltrán F J,Rivas J,Montero-de-Espinosa R.Catalytic ozonation of oxalic acid in an aqueous Ti O2slurry reactor[J].Applied Catalysis B:Environmental,2002,39(3):221-231.
[6]Jung H,Kim J W,Choi H,et al.Synthesis of nanosized biogenic magnetite and comparison of its catalytic activity in ozonation[J].Applied Catalysis B:Environmental,2008,83(3/4):208-213.
[7]Tong Shaoping,Liu Weiping,Leng Wenhua,et al.Characteristics of Mn O2catalytic ozonation of sulfosalicylic acid and propionic acid in water[J].Chemosphere,2003,50(10):1359-1364.
[8]lvarez P M,Beltrán F J,Pocostales J P,et al.Preparation and structural characterization of Co/Al2O3catalysts for the ozonation of pyruvic acid[J].Applied Catalysis B:Environmental,2007,72(3):322-330.
[9]Krishna K,Buenolopez A,Makkee M,et al.Potential rare earth modified Ce O2catalysts for soot oxidation:I.Characterisation and catllytic activity with O2[J].Applied Catalysis B:Environmental,2007,75(3/4):189-200.
[10]罗小涛,李金林.活性炭负载钴纳米催化剂的制备与表征[J].化学与生物工程,2010,27(8):24-27.
[11]Chen Honglin,Zhang Xiaoming,Feng Yujun,et al.Efficient degradation of fulvic acids in water by catalytic ozonation with Ce O2/AC[J].Journal of Chemical Technology&Biotechnology,2014,89(2):322-327.
[12]Faria P C C,Orfo J J M,Pereira M F R.A novel ceria-activated carbon composite for the catalytic ozonation of carboxylic acids[J].Catalysis Communications,2008,9(11/12):2121-2126.
[13]Avramescu S,Bradu C,Udrea I,et al.Degradation of oxalic acid from aqueous solutions by ozonation in presence of Ni/Al2O3catalysts[J].Catalysis Communications,2008,9(14):2386-2391.
[14]Staehelin J N M,Hoigne J.Decomposition of ozone in water in the presence of organic solutes acting as promoters and inhibitors of radical chain reactions[J].Environmental Science and Technology,1985,19(12):1206-1213.
[15]王列,姚玉元,孙利杰,等.活性炭纤维耦合柠檬酸铁在中性p H条件下活化双氧水降解染料[J].化学学报,2013,71(12):1633-1638.
[16]Faria P C C,Orfao J J M,Pereira M F R.Activated carbon catalytic ozonation of oxamic and oxalic acids[J].Applied Catalysis B:Environmental,2008,79(3):237-243.



